Joachim
Schulz
Photoelektronenspektroskopie
PES
Photoelektronenspektroskopie (PES) ist eine Methode zur Untersuchung der Struktur von Atomen, Molekülen und Feststoffen. Die Silbe Photo bedeutet dabei, dass eine Form von Licht verwendet wird, um Elektronen aus dem Versuchsobjekt herauszulösen. Zwar hat sichtbares Licht nicht genügend Energie um dies zu erreichen, aber bereits etwas kurzwelligere Strahlung, so genannte ultraviolette (UV) Strahlung, reicht aus um die am schwächsten gebundenen Elektronen zu lösen.
Ein Spektrum
Das folgende Bild zeigt ein Beispiel, wie ein Photoelektronenspektrum aussehen kann. Es ist das selbe Bild, dass ich auf der Seite zur Photoelektronenspektroskopie der Quantenwelt zeige und ist ein Spektrum von freien Atomen des Metalls Europium. Das Spektrum ist meiner Doktorarbeit entnommen:
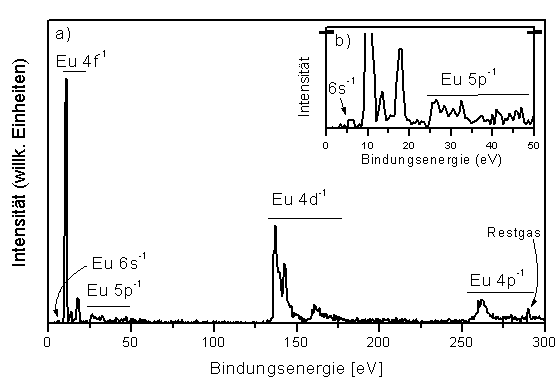
Auf der Grafik a) ist nach rechts die gemessene Energie aufgetragen, die man zum Auslösen der Elektronen braucht, und nach oben die Anzahl der Elektronen, die in einer bestimmten Zeit bei der entsprechenden Energie gemessen werden. Die Energie wird dabei oft in Elektronenvolt (eV) angegeben. Das ist die Energie, die ein Elektron aufnimmt, wenn es die Spannung von einem Volt durchläuft. Mit einer 12 V Autobatterie kann man Elektronen also auf 12 eV beschleunigen. Das Spektrum wurde mit Röntgenstrahlung einer Energie von über 300 eV aufgenommen. Zum Vergleich: Blaues Licht hat eine Energie von etwa 3 eV, rotes licht nur etwa 1,8 eV.
In dem Spektrum sieht man, dass etwa 6 eV nötig sind, um die am schwächsten gebundenen Elektronen herauszulösen. Diese Elektronen kann man im Orbitalmodell dem 6s-Orbital zuordnen. Die Intensität der 6s-Elektronen ist jedoch sehr schwach und kann am besten in der eingelegten Grafik b) gesehen werden. Zwischen 9 und 20 eV sind Elektronen aus den 4f-Orbitalen zu sehen. Hier erkennt man schon, dass das einfache Orbitalmodell nicht alles erklären kann: Das Spektrum enthält neben den grossen Hauptlinien auch kleinere, sogenannte Satelliten-Linien. Die Details des 4f-Spektrums sind vor allen deshalb interessant, weil diese Orbitale nur halb besetzt sind und daher viele sogenannte Umkopplungen der Elektronen untereinander möglich sind. Zudem tragen die 4f-Elektronen megnetische Felder, die für technische Anwendungen brauchbar sind. Im Anschluss an die 4f-Orbitale kommen sie vollständig besetzten 4p-Orbitale, die, wie die 6s-Elektronen, nur schwach zu sehen sind.
Stark gebunden sind erst die Elektronen, die zu inneren atomaren Schalen gehören. Von den inneren Schalen sind hier die 4d-Elektronen bei etwa 140 eV und die 4p-Elektronen bei mehr als 250 eV zu erkennen. Um die innersten Elektronen des 1s-Orbitals herauszulösen bräuchte man mehr als 48000 eV. Hierzu reichte die Energie in unserem Messaufbau nicht aus.
Technik
Die Aufnahme eines Photoelektronen-Spektrums ist mit vielen technischen Herausforderungen verbunden. So muss man zunächst die Atome in einem Zustand präparieren, in dem man sie untersuchen kann. Europium, dessen Spektrum ich hier zeige, ist ein Metall, das bei Zimmertemperatur fest ist. Es muss auf über 600 Grad erhitzt werden, damit genügend freie Atome im Gaszustand zur Verfügung stehen. Hierzu wird das Metall in einem speziellen Ofen verdampft. Die Verdampfung muss zudem im Luftleeren Raum (Vakuum) geschehen. Zum einen weil dass heisse Metall an der Luft verbrennen würde, zum anderen weil die Elektronen in der Luft mit Stickstoff- und Sauerstoffmolekülen zusammenstoßen würden, so dass man ihre Energie- und Winkelverteilung nicht mehr messen könnte. Unser Experiment befindet sich also vollständig in einem Edelstahlbehälter (Rezipient), dessen Innenraum mit hilfe mehrerer Vakuumpumpen bei einem extrem niedrigen Luftdruck gehalten wird. In unserem Fall bei deutlich weniger als dem hunderttausendsten Teil eines Millibars (10-5 mbar). Noch lieber messen wir bei einem Druck von wenigen 10-7 mbar. Je geringer der Druck ist, desto weniger wird das Spektrum durch Restgas, wie im Bild oben bei etwa 280 eV zu sehen, beeinträchtigt.
Das wichtigste Gerät zur Photoelektronen-Spektroskopie ist aber das Elektronenspektrometer. Dieses Gerät besteht mindestens aus einem Analysator, der Elektronen verschiedener Energie voneinander trennt, und einem Detektor, der die Elektronen misst und so für uns sichtbar macht. Oft gibt es zusätzlich noch eine Elektronenoptik, mit der die Elektronen gesammelt werden. Gegebenenfalls wird in dieser Optik auch die Energie der Elektronen in den für den Analysator optimalen Bereich verschoben. Alle Teile des Spektrometers müssen sich natürlich ebenfalls im Vakuum befinden.